前回のコラムから数回にわたり「糖鎖の自動合成」について取り扱っています。今回のコラムでは、化学合成法を技術基盤とした糖鎖自動合成装置を紹介します。 化学合成には、均一な溶液中で反応を行う液相合成、固相樹脂(レジン)上で反応を行う固相合成があります。液相で反応を行う場合は、反応、後処理、精製のステップで非常に労力、時間がかかります。固相で反応を行う場合は、後処理(洗浄)、精製のステップが非常に容易かつ迅速です。というのも樹脂はフィルターなどを通過しないため、フィルター付きチューブを使用すれば、反応後は溶媒でレジンを洗浄、精製することなく次の反応に進むことができるのです。すなわち、固相合成では樹脂上で目的とする化合物まで反応を続け、最終段階で樹脂から切り出し、最終物を精製することになります。 以上のことから、自動合成にはおのずと固相反応が向いていることになります。例えば、既に多くの自動合成装置が開発されているペプチド合成では、固相合成法が技術基盤となっています。ペプチド自動合成装置では、ビルディングブロックと言われるN端を Fmoc 基などで保護し、カルボン酸フリーの誘導体を樹脂に縮合、樹脂を溶媒洗浄、脱 Fmoc、樹脂を溶媒洗浄、ビルディングブロックを縮合・・・と、このサイクルを繰り返すことでアミノ酸を伸長させ、ペプチドを合成します(下図)。
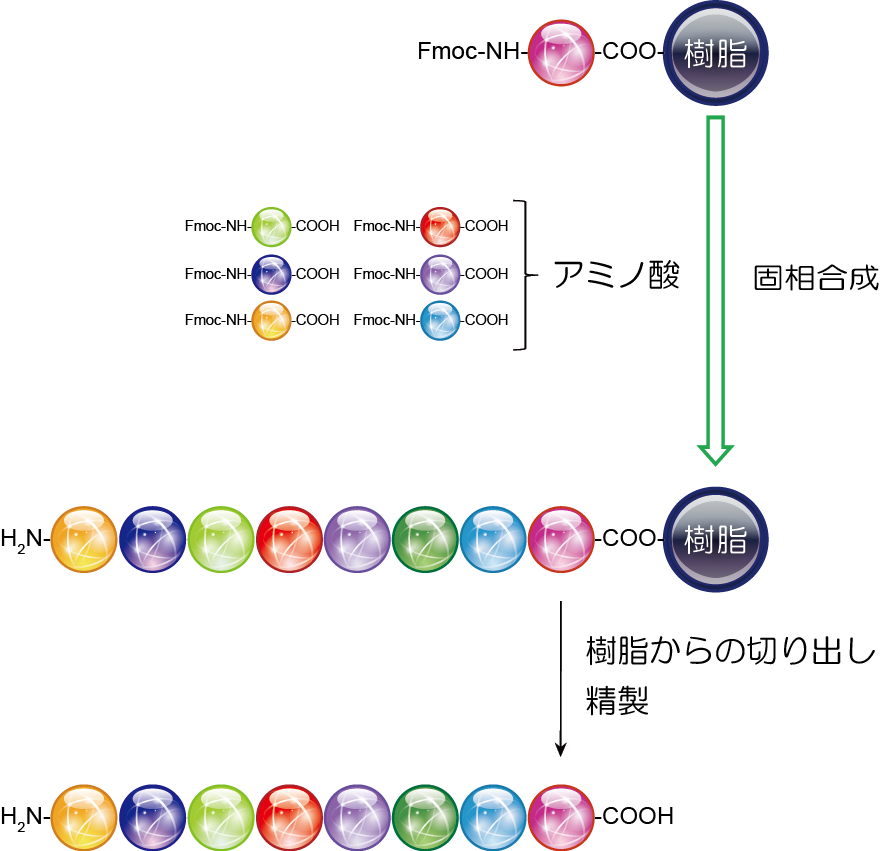
糖鎖では、化学合成を技術基盤とした自動合成装置でも、ペプチド合成と同様に樹脂を利用した固相合成法が採用されています。糖鎖の化学合成研究に携わった人であれば誰でも知っている Max Planck Institute の Prof. Dr. Peter H. Seeberger が、糖鎖の自動合成装置開発に勢力的に取り組んでおられます。先生らのグループでも固相を反応場として選択し、固相樹脂上でグリコシル化反応、脱保護、グリコシル化反応・・・のサイクルを繰り返すことで、種々の糖鎖自動合成を達成しています。しかしながら、これらの装置を使用すればどのような糖鎖でも合成できる、というわけではありません。以前のコラムでも紹介しましたが、グリコシル化反応では立体(α、β)を完璧に制御できる方法論は未だ存在しません。また、糖には1級水酸基(ヘキソースでは 6 位)と2級水酸基が存在し、1級水酸基の方が圧倒的に反応性が高く、立体障害も少ない(エキソサイクリック)性質を有し、2級水酸基は位置(ヘキソースでは 2 位、3 位、4 位)によっては反応(求核)性が極めて低いという性質があります。そのため、固相合成法で糖鎖を合成する場合、グリコシド結合の立体制御、グリコシル化反応収率を確保することが非常に困難となります。固相上でのグリコシル化反応を効率的に行うための研究は続けられていますが、どんな糖鎖合成にも対応可能な方法の開発には至っていません。ペプチド合成のアミノ酸ビルディングブロックでは、N端、側鎖のみを保護基で塞げば良いのですが、糖鎖合成では糖の複数の水酸基を適宜保護する必要があり、合成したい糖鎖結合位置にあわせて複数の糖ビルディングブロックを用意しなければなりません。すなわち、固相合成を実施するための材料(ビルディングブロック)を作る段階で、相当な労力を要します。化学合成法を基盤として糖鎖を自動合成できるようになるには、液相での糖鎖合成方法のさらなる発展、確立が必須であると言えます。 次回の糖鎖コラムでは酵素法を基盤とした糖鎖自動合成装置について紹介したいと思います。
弊社では、熟練した技術と豊富な経験、知識を持った研究員による受託解析サービス、合成サービスを実施しております。熟練した技術に基づく分析サンプル調製、HPLC、質量分析、NMR などの機器を駆使することで、種々の目的に応じた解析に対応しています。受託合成においては、蓄積した各種知見、ノウハウなどを駆使し様々なターゲットの合成実績がございます。まずはお気軽に御相談ください。ご予算に応じてベストなご提案をさせていただきます。

筆者プロフィール
naruken
博士(理学)北海道大学大学院理学研究科
専門:糖鎖工学、タンパク質工学、構造解析






