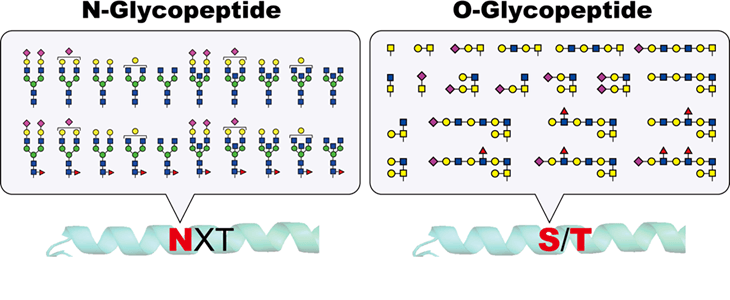
近年、世界でバイオ医薬品の開発が加速しており、2007年以降、バイオ医薬品は常に4品目以上が大型医薬品世界売上ランキング上位10品目に含まれています。バイオ医薬品にはインターフェロン、エリスロポエチンなどの「糖タンパク質医薬品」とヒュミラ、レミケード、ハーセプチンなどの「抗体医薬品」からなります。バイオ医薬品は細胞などで生産されることから、その生産宿主の翻訳後修飾をうけることになります。すなわち、糖鎖修飾であればN型糖鎖(アスパラギン側鎖)やO型糖鎖(セリン、トレオニン側鎖)が付加することになります。
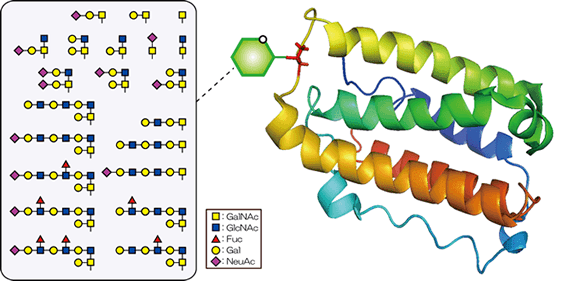
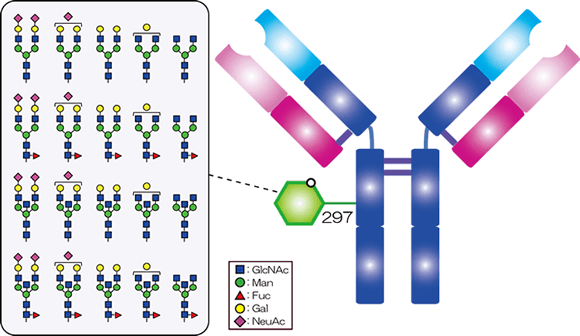
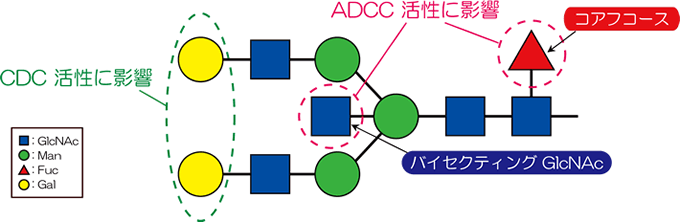
このような糖鎖修飾はバイオ医薬品の活性に影響を与える可能性があることから、厚生労働省は医薬審発第571号(平成13年5月1日)「生物薬品(バイオテクノロジー応用医薬品/生物起源由来医薬品)の規格及び試験方法の設定について」の構造解析・構造確認の項目において「糖組成・糖鎖構造」について言及しています。また、抗体については、薬食審査発1214第1号(平成24年12月14日)「抗体医薬品の品質評価のためのガイダンスについて」の特性解析の項目で糖鎖について詳しく指針がしめされています。抗体はH鎖のCH2ドメインにN結合型糖鎖が結合し、その糖鎖構造が抗体依存性細胞性細胞障害(Antibody-dependent cell-mediated cytotoxicity; ADCC)活性や補体依存性細胞障害(Complement-dependent cytotoxicity; CDC)活性に影響を与えることから糖鎖構造の詳細と主な糖鎖の不均一性について明らかにしなければなりません。
弊社では「タンパク質の品質管理」を解決する手段として、糖鎖受託解析サービスと糖ペプチド受託合成サービスでお客様のご要望にお応えいたします。
バイオ医薬品糖鎖受託解析
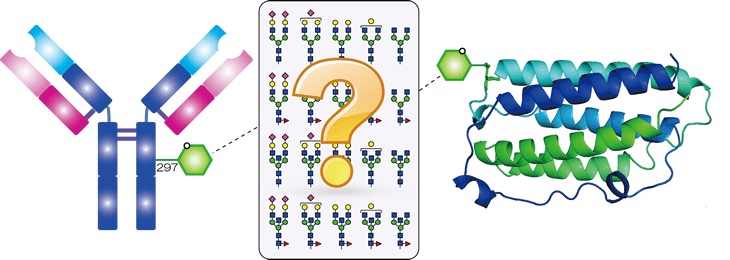
- バイオ医薬品の糖鎖プロファイルを明らかにします。
- 製造工程ごとの糖鎖プロファイルを把握することで、生産、精製方法の最適化が可能です。
- ロットの異なるサンプルを測定することで、ロット間差の把握し、製造工程管理にフィードバックできます。
解析の流れ
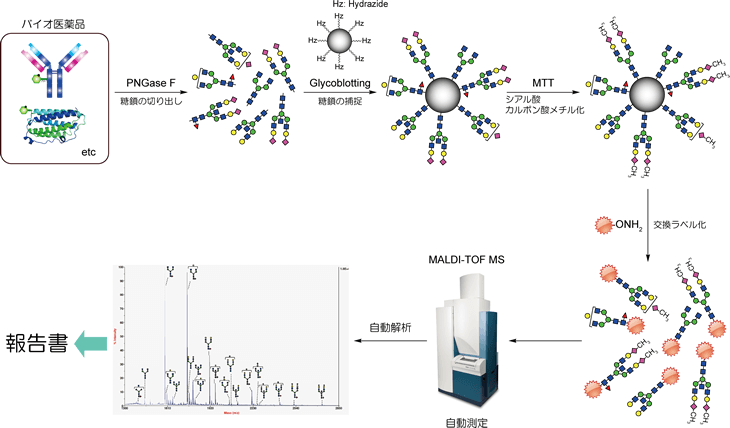
サンプル量:50 µg/検体
納期:2週間
糖ペプチド受託合成
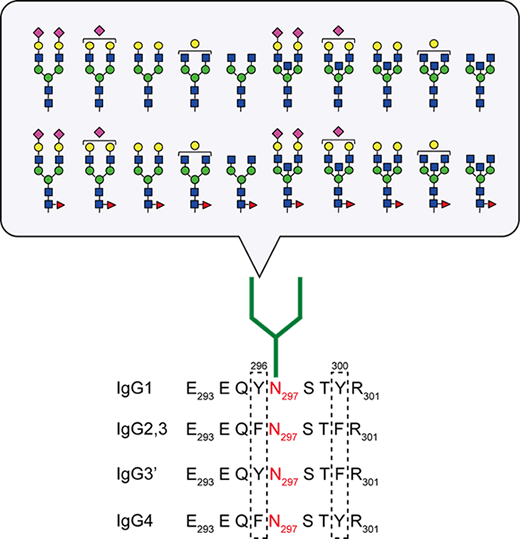
抗体医薬品として上市されている抗体はほとんどがIgGです。IgGにはサブクラスが1から4まで存在し、296残基目がチロシンかフェニルアラニン、300残基目がチロシンかフェニルアラニンかによって分類されています。また、IgGをトリプシンによって酵素分解すると下記に示すような断片が生じることが知られています。この断片の297残基目のアスパラギン側鎖はN結合型糖鎖が付加しています。
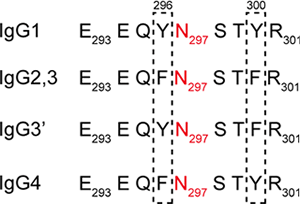
297残基目に結合しているN結合型糖鎖には下図のような様々な構造が存在します。
抗体医薬ではコアフコースが無い方がADC活性が高いなど、糖鎖の構造がその活性に大きな影響を与えます。
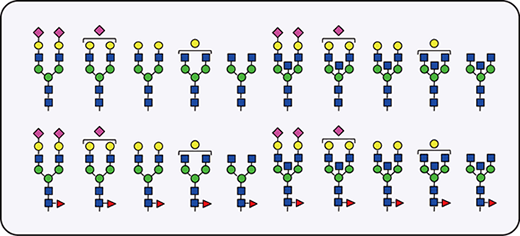
そのためトリプシン処理で生じるペプチド断片に相当する糖ペプチドは質量分析におけるMRM用標品や、ETD(or ECD)測定における重要な標準品となります。また、このような糖ペプチドは質量分析以外にも、HPLCやUPLCなどの高速液体クロマトグラフィーの標準品としても使用可能です。弊社では下図に示すような、トリプシン処理により生じるペプチド断片の297残基目に様々な2分岐型糖鎖構造を導入可能です。化学合成法と酵素法を適宜使用することで複雑な糖ペプチド合成に対応いたします。
抗体以外の糖タンパク質に由来するN結合型、O結合型糖ペプチド合成にも対応いたします。また、弊社ではO結合型糖ペプチドの固相合成に使用する糖アミノ酸ビルディングブロックを多数取り揃えており、多種多様な糖ペプチドの合成が可能となっています。